A 卷
开始测试
B 卷
二、综合题
11、BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验中,它是锗酸铋的简称。若知:①在BGO,锗处于其最高价态;②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈现的价态相同,在此氯化物中铋具有最外层8电子稳定结构;③BGO中可看成是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物所含氧的总质量相同。请填空:
(1)锗和铋的元素符号分别是________和________。
(2)BGO晶体的化学式是___________。
(3)BGO晶体中所含铋氧化物的化学式是_________。
[答案]
12、如图所示A、B、C、D、E变化关系,均省去了反应所需条件,
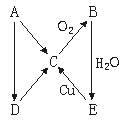
(1)如果A为气体单质,则:A_____________,B_____________,C_____________,D_____________,E_____________。
(2)如果A为固体单质,则:
A_____________,B_____________,C_____________,D_____________,E_____________。(均填分子式)
[答案]
13、实验室常用饱和NaNO2与NH4Cl溶液反应制取纯净氮气,反应式为:NH4Cl+NaNO2 NaCl+N2↑+2H2O,ΔH<0,实验装置如下图所示,试回答: NaCl+N2↑+2H2O,ΔH<0,实验装置如下图所示,试回答:
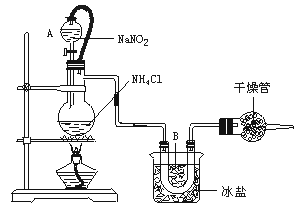
(1)装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是_________(填写编号)。
a.防止NaNO2饱和溶液蒸发
b.保证实验装置不漏气
c.使NaNO2饱和溶液容易滴下
(2)B部分的作用是_________。
a.冷凝 b.冷却氮气 c.缓冲氮气流
(3)加热前必须进行的一个操作步骤是__________________;加热片刻后,即应移去酒精灯以防反应物冲出,其原因是____________________________________。
(4)收集N2前,必须进行的操作步骤是(用文字说明)__________________。收集N2最适宜的方法是(填写编号)____________________________________。
a.用排气法收集在集气瓶中
b.用排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中
[答案]
14、如图所示,已知
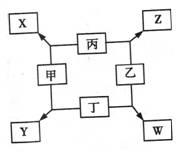
①甲、乙、丙、丁均为前三周期元素的单质。
②在一定条件下甲与丙和甲与丁都按物质的量之比1:3反应,分别生成X和Y,在产物中元素甲呈负价。
③在一定条件下乙与丙和乙与丁都按物质的量之比1:2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:
(1)甲是______________,乙是______________。
(2)甲与丙反应生成X的化学方程式是___________________________。
(3)乙与丁反应生成W的化学方程式是___________________________。
[答案]
15、已知氮的氧化物跟NaOH溶液发生的反应如下:
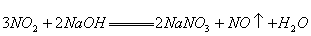
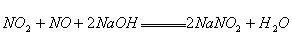
现有m mol的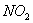 和n molNO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为 和n molNO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为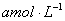 的NaOH溶液,求需此NaOH溶液的体积是多少? 的NaOH溶液,求需此NaOH溶液的体积是多少?
[答案]
|