A 卷
开始测试
B 卷
二、综合题
11、在氨水中存在如下平衡,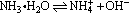 ,向该溶液中分别加入下列物质后,对上述平衡各有何影响?将答案填入表中。 ,向该溶液中分别加入下列物质后,对上述平衡各有何影响?将答案填入表中。

[答案]
12.在a、b两支试管中,分别装上形态相同、质量相等的一颗锌粒,然后向两支试管中分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。填写下列空白:
(1)a、b两支试管中的现象:相同点是_______________________;不同点是___________________;原因是________________________________。
(2)a、b两支试管中生成气体的体积开始是V(a)_______V(b);反应完毕后生成气体的总体积是V(a)______V(b);原因是____________________________________________。
[答案]
13.(1)在同体积c(H+)相同的盐酸、醋酸、稀硫酸溶液中分别加入足量的Zn与之反应,开始时放出H2的速率________(比较大小),充分反应后在相同条件下产生H2体积最大时是________。
(2)在同体积、同物质的量浓度的以上三种酸溶液里分别加入足量的Zn,开始反应时放出H2的速率由大到小的顺序是____________。
[答案]
14.H2S溶液中存在着H2S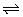 H++HS-、HS- H++HS-、HS-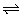 H++S2-的平衡。 H++S2-的平衡。
(1)当向H2S溶液中加入CuSO4溶液时,电离平衡向_________移动,c(S2-)______(填“增大”、“减小”或“不变”),c(H+)_______(填“增大”、“减小”或“不变”)。
(2)当向H2S溶液中加入少量NaOH固体时,电离平衡向_______移动,c(S2-)______(填“增大”、“减小”或“不变”),c(H+)_______(填“增大”、“减小”或“不变”)。
(3)当H2S溶液中加入少量Na2S固体时,电离平衡向______移动,c(S2-)______(填“增大”、“减小”或“不变”),c(H+)_______(填“增大”、“减小”或“不变”)。
(4)若将H2S溶液加热至沸,c(H2S)_________ (填“增大”、“减小”或“不变”);若要增大H2S溶液中c(S2-),最好加入__________。
[答案]
15、用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配成0.1 mol・L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是______________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH______________1(选填>,<,=);乙方案中,说明HA是弱电解质的现象是______________(填序号)。
a.装HCl溶液的试管中放出H2的速率快
b.装HA溶液的试管中放出H2的速率快
c.两个试管中产生气体速率一样快
(3)请你评价:乙方案中难以实现之处和不妥之处。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
[答案]
|