1、可逆反应N2+3H2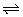 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
A.3v正(N2)=v正(H2)
B.v正(N2)=v逆(NH3)
C.2v正(H2)=3v逆(NH3)
D.v正(N2)=3v逆(H2)
2、在一定温度下,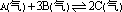 可逆反应达到平衡的标志是( )
可逆反应达到平衡的标志是( )
A.C生成的速率与C分解的速率相等
B.单位时间生成nmolA,同时生成3nmolB
C.A、B、C的浓度不再变化
D.A、B、C的分子数比为1:3:2
E.容器内的总压不随时间变化
3、在一密闭容器中,反应mA(g)  nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍,则()
nB(g)+nC(g)达平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,B和C的浓度均是原来的1.8倍,则()
A.平衡向逆反应方向移动了
B.物质A的转化率增加了
C.物质C的质量分数增加了
D.m<2n
4、能正确描述可逆反应:A(g)+2B(g)  2C(g)-热的图象是下列中的[V(A)%表示A在混和气体中的体积分数]()
2C(g)-热的图象是下列中的[V(A)%表示A在混和气体中的体积分数]()
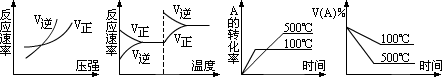
A
B
C
D
5、把NO2气体装入带活塞的圆筒中慢慢压缩,下列叙述正确的是()
A.体积减半,压强为原来二倍
B.体积减半,则NO2浓度减小
C.体积减半,N2O4的百分含量增大1倍
D.体积减半,压强增大,但小于原来的2倍
6、当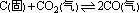 达到平衡后,为了取得更多的CO应采取的措施是(正反应为吸热反应)()
达到平衡后,为了取得更多的CO应采取的措施是(正反应为吸热反应)()
A.加压
B.使用催化剂
C.焦炭粉化
D.升温
7、如图所示,改变条件时,对反应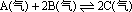 (正反应为放热反应)的影响情况,图中纵坐标Y表示()
(正反应为放热反应)的影响情况,图中纵坐标Y表示()