例1、(北京)对室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
A.加适量的醋酸钠晶体后,两溶液的pH均增大
B.使温度都升高20℃后,两溶液的pH均不变
C.加水稀释2倍后,两溶液的pH均减小
D.加足量的锌充分反应后,两溶液中产生的氢气一样多
答案:A
解析:
CH3COOH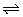 CH3COO-+H+,加入CH3COONa晶体,c(CH3COO-)增大,平衡向左移动,c(H+)减小,pH增大,CH3COONa+HCl=CH3COOH+NaCl,CH3COOH为弱电解质,c(H+)减小,pH增大,C错误;CH3COOH为弱电解质,pH相同的醋酸和盐酸溶液c(CH3COOH)>c(HCl), Zn+2HCl=ZnCl2+H2↑, Zn+2CH3COOH=(CH3COO)2Zn+H2↑,故CH3COOH溶液产生的H2较多,D错。 CH3COO-+H+,加入CH3COONa晶体,c(CH3COO-)增大,平衡向左移动,c(H+)减小,pH增大,CH3COONa+HCl=CH3COOH+NaCl,CH3COOH为弱电解质,c(H+)减小,pH增大,C错误;CH3COOH为弱电解质,pH相同的醋酸和盐酸溶液c(CH3COOH)>c(HCl), Zn+2HCl=ZnCl2+H2↑, Zn+2CH3COOH=(CH3COO)2Zn+H2↑,故CH3COOH溶液产生的H2较多,D错。
例2、将pH=1的盐酸平均分成两份,1份加适量水,另一份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为( )
A、9 B、10 C、11 D、12
答案:C
解析:
设原来HCl的体积为VmL。
若加水稀释时,耗用xmL水使溶液pH上升到2
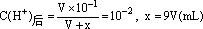
若加入NaOH反应,耗用ymL NaOH,使pH上升到2,则:
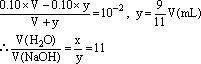
|