1、金属钠在空气中燃烧生成Na2O2和Na2O的混合物,取此燃烧产物7.48g溶于水制成1L溶液,取10mL用0.1mol·L-1的盐酸20mL恰好中和,可知该燃烧产物中Na2O的质量分数是( )
A.16.6% B.20.2%
C.80% D.78.4%
2、欲使每10个水分子中溶有1个Na+,则90mL水中应投入金属钠的质量为( )
A.10.5 g B.11.5g
C.21g D.23g
3、将x mol CO和y mol H2的混合气体充入盛有足量Na2O2的密闭容器中,再通入z mol O2,并用电火花使其充分反应,有关容器内反应的下列叙述不正确的是( )
A.参加反应的Na2O2为(x+y)mol
B.反应前后容器内压强之比(温度不变)为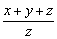
C.反应后容器中有O2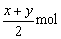
D.反应后生成了x mol Na2CO3和2 y mol NaOH
4、将3.72g由金属钠、氧化钠和过氧化钠组成的混合物与足量水反应。在标准状况下得到672mL混合气体。将该混合气体用电火花点燃,恰好完全反应,则原混合物中钠、氧化钠、过氧化钠的物质的量之比为( )
A.3︰2︰1 B.4︰2︰l
C.1︰1︰1 D.2︰1︰1
5、等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的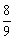 (同温同压)这时混合气体中N2、O2、CO2物质的量之比为( )
(同温同压)这时混合气体中N2、O2、CO2物质的量之比为( )
A.3︰4︰1 B.3︰3︰2
C.6︰7︰3 D.6︰9︰0
6、取a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g。下列物质中不能满足上述结果的是( )
A.H2 B.CO
C.C6H12O6 D.C12H22O11
7、某二价金属碳酸盐和碳酸氢盐的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为6︰5,该混合物中碳酸盐和碳酸氢盐的物质的量之比为( )
A.1︰1 B.1︰2
C.1︰3 D.1︰4
8、同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,允分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V3>V1>V2
9、某100mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4 mol·L-1、0.1 mol·L-1,向该混合液中加入1.92g Cu粉,加热,待充分反应后,所得溶液中的Cu2+物质的量浓度是( )
A.0.15mol·L-1 B.0.225 mol·L-1
C.0.35 mol·L-1 D.0.45 mol·L-1
10、当镁与某浓度的硝酸反应时,若参加反应的Mg与HNO3的物质的量之比为2︰5,则硝酸的还原产物可能是( )
A.NO B.NO2
C.N2O D.NH4NO3
11、将8.4g Fe溶于一定量稀硝酸中,完全反应后,n(Fe2+)=n(Fe3+),则稀硝酸中含HNO3( )
A.0.125mol B.0.25mol
C.0.375mol D.0.5mol
12、铜与lmol·L-1稀HNO3反应,如果NO3-浓度下降0.2mol·L-1,则溶液中(H+)的浓度同时下降( )
A.0.8mol·L-1 B.0.6mol·L-1
C.0.4mool·L-1 D.0.2mol·L-1
13、铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL N2O4气(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
A.9.02g B.8.51g
C.8.26g D.7.04g
14、a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、蒸干灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为( )
A.70% B.52.4%
C.47.6% D.30%
15、将一定质量的Mg,Zn,Al混合物与足量稀H2SO4反应,生成H2 2.8L(标准状况),原混合物的质量可能是( )
A.2g B.4g
C.8g D.10g
16、今有一含NaHCO3 16.8g的稀溶液(无其它溶质),若向其中加入某给定的物质,可将其恰好转化为只含有Na2CO3 21.2g的水溶液。有多种物质均可满足“给定的物质”的条件。请完成下列各小题:
(1)你从课本知识中学到的能够满足给定条件的物质就有四种,其中有两种在反应过程中还有气体产生。它们是:①________②________③________④________(填化学式且排序不分先后)
(2)在实现上述的转化过程中,溶液中碳元素的质量均________(填“增加”、“不变”或“减少”)
(3)在(1)中填写的各种物质中,其中有一种物质在反应过程中只需一步反应就可以只生成Na2CO3和水。其化学方程式为:________________________________________
(4)在(1)中填写的各种物质中,其中有一种物质在反应过程中有可燃性气体生成。如果满足条件需要该物质________g。
17、气体A由C、H、F、S中的三种元素组成。将标准状况下1.12L气体A在过量的O2中完全燃烧,恢复到原状态,放出Q kJ的热量。已知气态生成物全部被过量的澄清石灰水吸收,可以得到6.95g沉淀。再取相同状况下的1.12L气体A装入一个薄膜袋里,袋和气体的总质量为2.20g。(已知CaSO3、CaF2、CaCO3常温下难溶于水)
(1)根据上述数据估算,A的相对分子质量不会大于________。
(2)通过计算、分析可确定A的化学式为________________。
(3)薄膜袋的质量为________。
(4)写出该条件下A在O2中燃烧的热化学方程式:________________________。
20、将一块铜板浸泡在一定浓度的FeCl3溶液中一段时间后取出,得到一混合溶液,某校化学兴趣小组的同学为分析该混合溶液的组成,进行了如下实验:
Ⅰ.取50.0mL混合溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为86.1g;
Ⅱ.另取50.0mL混合溶液,向其中加入1.40g铁粉,结果铁粉全部溶解但未见固体析出;
Ⅲ.再取50.0mL混合溶液,向其中加入20.0mL稀硝酸,得到一种无色气体,其体积换算成标准状况时为0.448L。
请根据以上实验中得到的数据分析计算:
(1)原FeCl3溶液物质的量浓度(反应过程中溶液体积的变化忽略不计);
(2)所得混合溶液中c(Cu2+)的取值范围;
(3)若要进一步求得混合溶液中c(Cu2+)的具体数值,在只单独使用AgNO3溶液、铁粉或稀硝酸的前提下,还可测出哪些数据,必须进行哪些实验?