1����(Bi)��ҽҩ��������ҪӦ�á����й���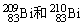 ��˵����ȷ����������
��˵����ȷ����������
A��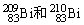 ������83������
������83������
B��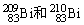 ��Ϊͬλ��
��Ϊͬλ��
C��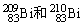 �ĺ����������ͬ
�ĺ����������ͬ
D��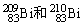 �ֱ���126��127������
�ֱ���126��127������
2�����п����ڲⶨ��ҺpH�Ҿ�ȷ����ߵ���������
A�����ָʾ������������������B��pH��
C������pH��ֽ����������������D���㷺pH��ֽ
3�����з��ϻ�ѧʵ�顰��ɫ��������������
������ȡ��������ʾʵ���У���CCl4��ȡ��ˮ��ΪCCl4��ȡ��ˮ������ͭ��Ũ���ᷴӦ��ʵ���У���ͭƬ��Ϊ�ɵ��ڸ߶ȵ�ͭ˿���۽�ʵ���ҵķ���Һ��ϼ�Һ�кͺ����ŷ�
A���٢ڡ���������������������B���٢�
C���ڢۡ���������������������D���٢ڢ�
4����ѧ�ҽ��������Ƴ�һ������ϸ��ȼ�ϵ�أ�����ϸ�����л���ת������������������������Ϊ����ʵ�ȼ�ϵ�ط��硣��ظ�����ӦΪ������
A��H2��2OH��=2H2O��2e��
B��O2��4H����4e��=2H2O
C��H2=2H����2e��
D��O2��2H2O��4e��=4OH��
5������ʵ�������ȫ��ȷ����������
��� |
ʵ�� |
���� |
A |
����ˮ�ķ�Ӧ |
�����Ӵ�ú����ȡ�������ƣ������̶���С���ƣ�С�ķ���װ��ˮ���ձ��� |
B |
����һ��Ũ�ȵ��Ȼ�����Һ1000mL |
ȷ��ȡ�Ȼ��ع��壬���뵽l000mL������ƿ�У���ˮ�ܽ⣬��ҡ�ȣ����� |
C |
�ų���ʽ�ζ��ܼ��첿�ֵ����� |
����������ʹ��������б���ϣ�����ָ��ס���ܣ����ἷѹ�����飬ʹ��Һ�Ӽ������� |
D |
ȡ����Һ©����������ϲ�Һ�� |
�²�Һ��ӷ�Һ©���¶˹ܿڷų����رջ�������һ�������������ϲ�Һ������ӷ�Һ©���¶˹ܿڷų� |
6��Ϊ�˱�����ͭ������ͭ�̣����·�����ȷ����������
A������ͭ����������������
B������ͭ�������ڸ���Ļ�����
C������ͭ�������ڳ�ʪ�Ŀ�����
D������ͭ���ı��渲��һ������ĸ߷���Ĥ
7��˳ʽPt(NH3)2Cl2(ʽ��Ϊ300)���ٴ��㷺ʹ�õĿ�����ҩ������йظ����ʵ�˵����ȷ����������
A����4��Ԫ�����
B������NH3����
C��Pt�Ļ��ϼ�Ϊ��4
D��PtԪ�ص������ٷֺ���Ϊ65%
8����V1 mL 1.00mol��L��1HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ��������ͼ��ʾ(ʵ����ʼ�ձ���V1��V2=50mL)������������ȷ����������
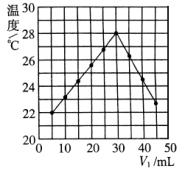
A������ʵ��ʱ�����¶�Ϊ22��
B����ʵ�������ѧ�ܿ���ת��Ϊ����
C��NaOH��Һ��Ũ��Լ��1.00mol��L��1
D����ʵ�������ˮ���ɵķ�Ӧ���Ƿ��ȷ�Ӧ
9�������±������ķ���ʽ���й��ɣ��жϿո�������ͬ���칹����Ŀ��������
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
CH4 |
C2H4 |
C3H8 |
C4H8 |
�� |
C6H12 |
C7H16 |
C8H16 |
A��3������������������������ B��4
C��5������������������������ D��6
10�����г�ȥ���ʵķ�����ȷ����������
�ٳ�ȥ��������������ϩ������������ͨ��Cl2����Һ���룻
�ڳ�ȥ��������������������ñ���̼��������Һϴ�ӣ���Һ���������
�۳�ȥCO2��������SO2������ͨ��ʢ����̼������Һ��ϴ��ƿ��
�ܳ�ȥ�Ҵ��������������������ʯ�ң�����
A���٢ڡ���������������������B���ڢ�
C���ۢܡ���������������������D���ڢ�
11�����������������������
A��13C��14C����ͬһ��Ԫ�أ����ǻ�Ϊͬλ��
B��1H��2H�Dz�ͬ�ĺ��أ����ǵ����������
C��14C��14N����������ȣ����ǵ�����������
D��6Li��7Li�ĵ�������ȣ�������Ҳ���
12��a g�����뺬��H2SO4��CuSO4��Һ��ȫ��Ӧ�õ�a gͭ������뷴Ӧ��CuSO4��H2SO4�����ʵ���֮��Ϊ������
A��1�U7����������������������B��7�U1
C��7�U8����������������������D��8�U7
13��һ�������£��ϳɰ���Ӧ�ﵽƽ��ʱ����û�������а������������Ϊ20.0%���뷴Ӧǰ�������ȣ���Ӧ�������С�İٷ�����������
A��16.7%�������������������� B��20.0%
C��80.0%�������������������� D��83.3%
14�����Ӽ���ij��÷��������֣�
���鷽�� |
������ |
��ɫ�� |
���巨 |
���� |
��Ӧ���г����������ܽ� |
��Ӧ������ɫ�仯 |
��Ӧ����������� |
�������Ӽ���ķ�������������������
A��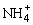 �������巨����������B��I������������
�������巨����������B��I������������
C��Fe3��������ɫ������������D��Ca2���������巨
15���й�����ȼ��ʱ������ɫ�����������������
A��������������ȼ�ա�����ɫ
B�����ڿ�����ȼ�ա�����ɫ
C���Ҵ��ڿ�����ȼ�ա�������ɫ
D������������ȼ�ա�����ɫ
16����һ���ѳ�ȥ��������Ĥ�����������������Թ����(����ͼ)�����Թܽ������ṯ��Һ�У�Ƭ��ȡ����Ȼ�����ڿ����У���������������������ë������īˮ���Ҷ�����������ʵ�������ж�����˵���������������
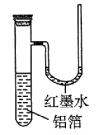
A��ʵ���з����ķ�Ӧ����������ԭ��Ӧ
B������һ�ֽϻ��õĽ���
C������������Ӧ�ų�����������
D����Ƭ�����ɵİ�ë�����������������Ļ����
18����֪ϡ��ˮ���Ȼ�����Һ���ʻ�ɫ��������������ϡ�Ȼ�������Һ�У�����l��2��Һ�壬����Һ�ʻ�ɫ��
����(1)��ͬѧ��Ϊ�ⲻ�Ƿ�����ѧ��Ӧ���£���ʹ��Һ�ʻ�ɫ�������ǣ�__________(�����ӵĻ�ѧʽ����ͬ)��
������ͬѧ��Ϊ���Ƿ�����ѧ��Ӧ���£���ʹ��Һ�ʻ�ɫ��������__________��
����(2)����Ϊ��λͬѧ�Ĺ۵�����ȷ��? __________ (��ס����ҡ�)��Ϊ����֤����жϵ���ȷ�ԣ�������������ṩ�Ŀ����Լ��������ַ���������֤������ѡ�õ��Լ����ż�ʵ���й۲쵽�����������±���
����ʵ��ɹ�ѡ���Լ���
����A�����Ը��������ҺB������������ҺC�����Ȼ�̼D�����軯����ҺE����������ҺF�����۵⻯����Һ
ʵ�鷽�� |
��ѡ���Լ�(�����) |
ʵ������ |
����һ |
�� |
�� |
������ |
�� |
�� |
����(3)��������ʵ���Ʋ⣬����ϡ�廯������Һ��ͨ�������������ȱ�������������__________����ѡ�õ��۵⻯����Һ���ж���λͬѧ���ƶ�����ȷ�ģ�����Ϊ�Ƿ����? __________�������ǣ�____________________��
����(4)�ڱ�״���£�����100.0mL�廯������Һ��ͨ��268.8mL Cl2ʱ��70%���屻��������ԭ�廯������Һ�����ʵ���Ũ��Ϊ__________mol��L��1����������Ӧ�����ӷ���ʽΪ��__________��
20���ش�ʵ������ȡNH3�����а�������ʵ����������⣬����Ҫ����д�հס�
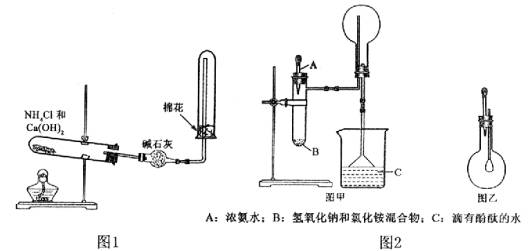
����(1)ʵ������ͼ1��ʾװ���Ʊ������NH3��
�����ٷ�Ӧ�Ļ�ѧ����ʽΪ��____________________��װ�����ռ�NH3���Թܿڷ������ŵ������ǣ�____________________��
�����ڸ�����и�����ܷ������ˮCaCl2__________��������____________________��
����(2)ͼ2��ij��ѧС���Ʊ�NH3����������ʵ��ʱ�ĸĽ�װ�á���ͼ�װ�������װ�ã���ȡ2g�����Ȼ��װ���Թܵײ����ٿ��ٳ�ȡ2g�������Ƹ������Ȼ����Ϸ��������ô��еιܵ���������(�ι�Ԥ������Լ2mLŨ��ˮ)���ձ���ʢ���з�̪��Һ��ˮ����Ũ��ˮ�����Թ���������۲쵽�Թ��ڷ������ҷ�Ӧ���д������ݲ�����
������ͼ��������NH3��Բ����ƿȡ�£���װ��ͼ����ʾ��װ�ã���ͷ�ι�����������2mL H2O����ʱС����ϵ�ڲ������ϳ���Ȼ�ɳ�״̬�����ι��ڵ�ˮ����������ƿ�У�����ζ���ƿ��ͨ���۲�ʵ������������֤NH3��ij�����ʡ�
������������ijͬѧ����ij��ѧС������ͼ����ȡNH3��ԭ��������е�������____________________��
����a����NH3��H2O����ƽ�⣺NH3��H2O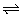 NH3��H2O
NH3��H2O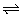 NH4����OH����NaOHʹƽ�������ƶ�
NH4����OH����NaOHʹƽ�������ƶ�
����b����NH3��H2O����ƽ�⣺NH3��H2O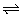 NH3��H2O
NH3��H2O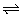 NH4����OH����NH4Clʹƽ�������ƶ�
NH4����OH����NH4Clʹƽ�������ƶ�
����c��NaOH����ˮʱ���ȣ�ʹ��ϵ���¶����ߣ�NH3���ܽ�ȼ�С�����в���NH3�ݳ�
����d��NH4Cl��NaOH�ڴ�����¿ɷ�Ӧ����NH3����NH4����OH��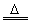 NH3����H2O
NH3����H2O
����e��NH4Cl��ֽ��ͷų�NH3
������ͼ���е�NH4Cl��NaOH���������ܷ���CaO�������? __________(��ܡ����ܡ�)��
����������ж�ͼ������ƿ������NH3? __________��
������ͼ�����潺ͷ�ι��е�ˮ������ƿ�У��۲쵽��������__________��˵��NH3__________��