1��̼����(SiC)��һ�־��壬�������ƽ��ʯ�Ľṹ������̼ԭ�Ӻ�ԭ�ӵ�λ���ǽ���ġ����������־���ٽ��ʯ���ھ���裬��̼�����У����ǵ��۵�Ӹߵ��͵�˳����������
A���٢ۢڡ�������������������B���ڢۢ�
C���ۢ٢ڡ�������������������D���ڢ٢�
2�����ۼ������Ӽ������Ӽ��������ܹ������ʵ����Ӽ�IJ�ͬ������������������˵�������������ľ�����������
A��CCl4���塡����������������B��SiO2����
C��NaOH���塡����������������D��K2O����
3��NaF��NaI��MgO��Ϊ���ӻ���������������ݣ������ֻ�������۵�ߵ�˳����������
����ʡ���������NaF������������NaI��������������MgO
���ӵ������������1��������������1����������������2
����/10��10m����2.31������������3.18������������2.10
A���٢ڢۡ�������������������B���ۢ٢�
C���ۢڢ١�������������������D���ڢۢ�
4�����о����������ȷ��һ����������

|
���Ӿ��� |
ԭ�Ӿ��� |
���Ӿ��� |
A |
NaOH |
Ar |
SO2 |
B |
H2SO4 |
ʯī |
S |
C |
NaCl |
SiO2 |
|
D |
Ba(OH)2 |
���ʯ |
���� |
5��ij���ʵľ����к�A��B��C����Ԫ�أ������з�ʽ����ͼ��ʾ(����ǰ���������ϵ�Bԭ��δ����)��������A��B��C��ԭ�Ӹ���֮������Ϊ������
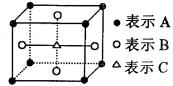
A��1�U3�U1������������������ B��2�U3�Ul
C��2�U2�Ul������������������ D��1�U3�U3
6��HgCl2��ϡ��Һ������������������������֪HgCl2���۵���277�棬����״̬��HgCl2���ܵ��磬HgCl2��Һ�����ĵ��������������й���HgCl2����������ȷ����������
��HgCl2���ڹ��ۻ������HgCl2���������Ӿ��塡��HgCl2���ڷǵ���ʡ���HgCl2�����������
A���٢ۡ���������������������B���٢�
C���ڢۡ���������������������D���ڢ�
7����ʯī�����У�ÿһ����������̼ԭ�ӹ��������������νṹ����ƽ��ÿ������������ռ�е�̼ԭ�Ӹ���Ϊ������
A��6������������������������ B��4
C��3������������������������ D��2
8�����е���ʽ����ȷ����������
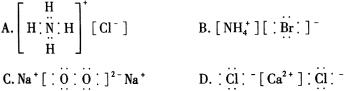
9�����з��ӵĽṹ�У�����ԭ�ӵ��������Ӷ�����8�����ȶ��ṹ����������
A��BF3���������������������� B��H2O
C��SiCl4�������������������� �� D��PCl5
10������������ȷ����������
A�����Ǽ��Լ��ķ��Ӳ�һ���ǷǼ��Է���
B���Լ��Լ���������ķ���һ���Ǽ��Է���
C���Ǽ��Լ�ֻ������˫ԭ�ӵ��ʷ�����
D���Ǽ��Է����У�һ�����зǼ��Թ��ۼ�
11�����������������������������
A����������
B�����»���
C�����ۼ�
D�����������Ӻ����ɵ��Ӽ�ǿ�ҵ������
12�����ھ��������˵������ȷ����������
A�����ǽ����ض�����������
B���ھ�����ֻҪ�������Ӿ�һ����������
C�����Ӿ�����۵�һ���Ƚ�������ĵ�
D��ԭ�Ӿ�����۵�һ���Ƚ�������ĸ�
13����ȷ��������ͨ�Ե���������
A�����н�����������������B������������չ�ԡ����絼��
C�����и��۵㡡��������������D�����û����е���
14��ij��������״̬�ɵ��磬��̬�ɵ��磬����Ͷ��ˮ�к�ˮ��ҺҲ�ɵ��磬����Ʋ�����ʿ�����������
A����������������������������B���ǽ���
C�������Լ����������������D����������
15�������йؽ���Ԫ����������������ȷ����������
A������ԭ��ֻ�л�ԭ�ԣ�����������ֻ��������
B������Ԫ���ڻ�������һ���������ϼ�
C������Ԫ���ڲ�ͬ�������л��ϼ۾�����ͬ
D������Ԫ�صĵ����ڳ����¾�Ϊ����
16����Ԫ���ж��ּ�̬�������γɶ��ֺ���������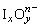 ����2��
����2��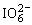 �������干��һ�����γɵ�
�������干��һ�����γɵ�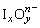 �Ļ�ѧʽΪ������
�Ļ�ѧʽΪ������

17��ʯī�������ڵĽ��������ã��γ�ʯī��϶�����Kԭ�������ʯī����̼ԭ���У��Ƚϳ�����ʯī��϶����������ͭɫ�Ļ�����仯ѧʽΪCxK����ƽ��ͼ�μ�ͼ����x��ֵΪ������
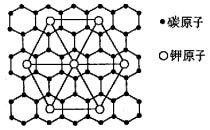
A��8���������������������� B��12
C��24����������������������D��60