A 卷
开始测试
B 卷
二、综合题
11、三位学生设计了下述三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确证试液中的SO42-。
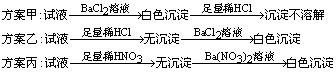
试评价上述各种方案是否严密,并分别说明理由。
[答案]
12 、在下列用途或反应中,硫酸表现出的性质为:A、高沸点性;B、强酸性;C、吸水性;D、脱水性;E、强氧化性。试用字母填空:
(1)实验室制取氢气:________;
(2)实验室制取HCl气体:________;
(3)干燥二氧化硫:________;
(4)浓硫酸溶解金属银:________;
(5)浓硫酸可用钢瓶贮运:________;
(6)生产过磷酸钙化肥:________;
(7)浓硫酸可使湿润的蓝色石蕊试纸先变红,后变黑:________;
(8)将浓硫酸加到浓盐酸中产生白雾:________。
[答案]
13 、过二硫酸钾(K2S2O8)在高于100℃的条件下发生反应,其化学方程式为:
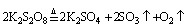 。 。
现称取一定质量的K2S2O8固体(含有不分解的杂质)进行如下实验:加热使过二硫酸钾完全分解,通过测定氧气的体积计算过二硫酸钾的纯度,并且收集三氧化硫,进行观察和检验。
(1)试从下图中选用几种必要的装置,连接成一整套实验装置。这些选用装置的接口编号连接顺序是________。
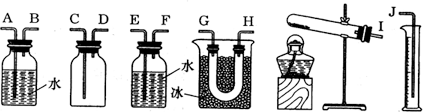
(2)观察到的三氧化硫的颜色和状态是_______。将三氧化硫与水反应,鉴定反应产物中阴离子的方法是________。
(3)若实验时称取过二硫酸钾的质量为Wg,测得氧气的体积(折算成标准状况)为a mL,则此过二硫酸钾的纯度为_________。
[答案]
14、溶液中可能有下列阴离子中的一种或几种:SO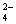 、SO 、SO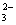 、CO 、CO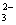 、Cl-. 、Cl-.
(1)当溶液中有大量H+存在时,则不可能存在______.
(2)当溶液中有大量Ba2+存在时,则不可能存在______.
(3)当溶液中有_________和_________阳离子存在时,上述所有阴离子都不可能存在.
(4)当向溶液中通入足量Cl2时,______离子在溶液中不能存在.
[答案]
15、从某物质A的水溶液出发有下图所示的一系列变化:
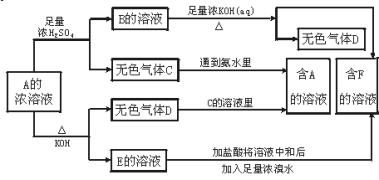
试回答:
(1)物质的化学式:A__________,B__________,C__________,D__________,E__________,F__________.
(2)写出E→F的离子方程式______________________________________.
(3)鉴定物质F的方法______________________________________________________.
[答案]
|