A 卷
开始测试
B 卷
二、综合题
11、下图是某学生设计的验证氯气有无漂白作用与制取饱和氯水的实验装置,试回答下列问题:
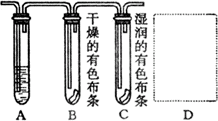
(1)装置A中溶液是___________,其作用是___________;
(2)装置B、C中的实验现象是______________________,由此得出的结论是______________________;
(3)在方框D中,画出制取饱和氯水的实验装置图。
[答案]
12、实验室里用所给仪器(如图)组装实验装置制备纯净的无水CuCl2。回答下列问题:
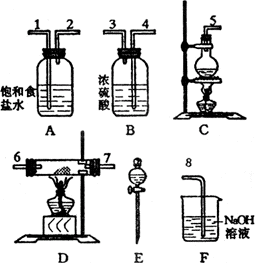
(1)组装氯气发生装置,应选用的仪器是___________,E的名称是___________。
(2)按Cl2气流方向,其余装置的连接顺序(用数字1、2、…填入)是:( )→( )→( )→( )→( )→( )→( )→( )
(3)实验前检查整套装置的气密性的方法是:__________________________________________。
(4)装置A的作用是___________,装置B的作用是___________。
(5)装置F的烧杯中盛___________(名称),其作用是___________,反应方程式是______________________。
(6)待充分反应后,装置D的玻璃管中剩余物呈___________色,将制得的产物配制成饱和溶液,呈___________色
[答案]
13、有X、Y、Z三种常见元素,已知:
①X、Y、Z单质在通常情况下均为气体;
②X单质可在Z单质中燃烧火焰呈苍白色,反应生成化合物XZ
③XZ易溶于水,其水溶液可使蓝色石蕊试纸变红
④X2和Y2在一定条件下能化合生成X2Y,X2Y在常温下为无色液体
⑤Z单质可溶于X2Y所得溶液具有漂白作用
据此推断分析:
(1)X为_________,Y为_________,Z为________(填元素名称)
(2)反应生成物的化学式:XZ为___________,X2Y为___________
(3)反应②的化学方程式为______________________。
[答案]
14、下列装置图中,A是氯气的发生装置,B中盛水,C中盛浓硫酸;D中装铜丝网;反应后E的底部有棕黄色固体聚集;F是吸收多余气体的装置。
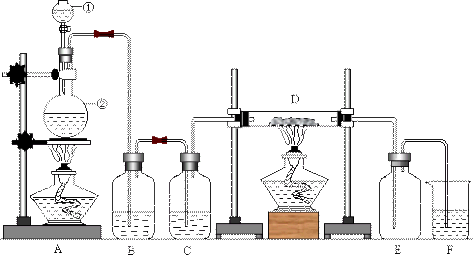
(1)写出所标仪器的名称:①__________,②__________。在这两个仪器中分别装入的药品是①____________,②____________。
(2)仪器①能否换成长颈漏斗,________________,原因是________________________________________。
(3)B装置的用途是________________________________;
C装置的用途是________________________________________。
(4)实验室制取Cl2的方程式为________________________,所用药品可选用①MnO2;②稀盐酸;③浓盐酸;④KMnO4;⑤KClO3;⑥NaCl;⑦浓H2SO4;⑧Ca(ClO)2中的( )
A、①③ B、①② C、③④
D、③⑦ E、①⑥⑦
[答案]
15、(江苏)较低温度下,氯气通入石灰乳中可制得漂白粉,该反应为放热反应。某校甲、乙两化学研究性学习小组均用200 mL 12 mol / L盐酸与17.4 g MnO2在加热条件下反应制备氯气,并将制备的氯气与过量的石灰乳反应制取漂白粉,用稀氢氧化钠溶液吸收残余的氯气。分析实验结果发现:① 甲、乙两组制得的漂白粉中Ca(ClO)2的质量明显小于理论值,② 甲组在较高温度下将氯气与过量的石灰乳反应,所制得的产品中Ca(ClO3)2的含量较高。试回答下列问题:
(1)上述实验中理论上最多可制得Ca(ClO)2多少克?
(2)实验中所得到的Ca(ClO)2的质量明显小于理论值,试简要分析其可能原因,并写出可能涉及到的化学方程式。 [答案]
|