ЁЁ1ЁЂВЛЭЌЮяжЪМфЕФбѕЛЏЛЙдЗДгІ
ЁЁЁЁЃЈ1ЃЉШЋВПбѕЛЏЛЙдЗДгІЃЈБфМлдЊЫиЕФЫљгадзгЕФМлЬЌЗЂЩњБфЛЏЃЉ
ЁЁЁЁЁЁ
ЁЁЁЁ
ЁЁЁЁЃЈ2ЃЉВПЗжбѕЛЏЛЙдЗДгІЃЈБфМлдЊЫиЕФдзгжЛгаВПЗжМлЬЌЗЂЩњБфЛЏЃЉ
ЁЁЁЁЁЁ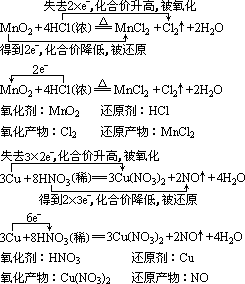
ЁЁ2ЁЂЭЌвЛЮяжЪФкВЛЭЌдЊЫиМфЕФбѕЛЏЛЙдЗДгІ
ЁЁЁЁЁЁ
ЁЁЁЁЁЁ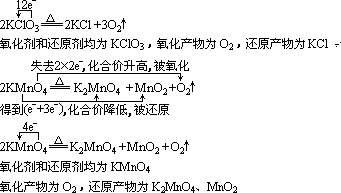
ЁЁ3ЁЂСНжжвдЩЯдЊЫиМфЕФбѕЛЏЛЙдЗДгІ
ЁЁЁЁЃЈ1ЃЉвЛжждЊЫибѕЛЏСНжждЊЫи
ЁЁЁЁЁЁ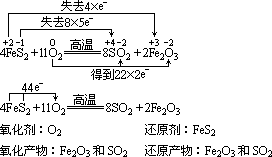
ЁЁЁЁЃЈ2ЃЉвЛжждЊЫиЛЙдСНжждЊЫи
ЁЁЁЁЁЁ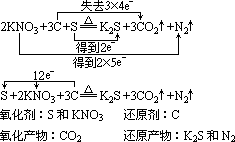
ЁЁ4ЁЂЭЌжждЊЫиМфЕФбѕЛЏЛЙдЗДгІ
ЁЁЁЁЃЈ1ЃЉЦчЛЏЗДгІЃКЭЌвЛЮяжЪжаЭЌжжМлЬЌЕФЭЌвЛдЊЫиЕФЛЏКЯМлВПЗжЩ§ИпЁЂВПЗжНЕЕЭЕФЗДгІЁЃ
ЁЁЁЁЁЁ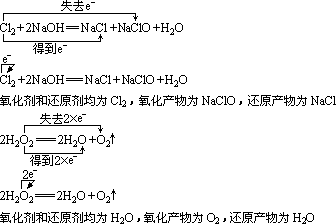
ЁЁЁЁЃЈ2ЃЉЙщжаЗДгІЃКВЛЭЌМлЬЌЕФЭЌвЛдЊЫиЖМзЊЛЏЮЊЭЌвЛЛЏКЯМлИУдЊЫиЕФЗДгІЁЃ
ЁЁЁЁЁЁ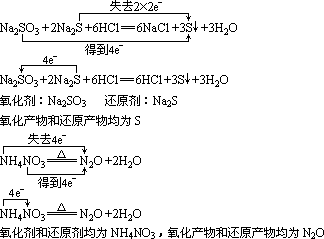
ЁЁЁЁЃЈ3ЃЉЦфЫќЗДгІ
ЁЁЁЁЁЁ
ЃЈЖўЃЉбѕЛЏадКЭЛЙдадЧПШѕЕФХаЖЯЗНЗЈЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ1ЁЂИљОнН№ЪєЛюЖЏадЫГађНјааХаЖЯ
ЁЁЁЁЁЁ
ЁЁ2ЁЂИљОнЗДгІЗНГЬЪННјааХаЖЯ
ЁЁЁЁ бѕЛЏадЃКбѕЛЏМСЃОбѕЛЏВњЮя
ЁЁЁЁ ЛЙдадЃКЛЙдМСЃОЛЙдВњЮя
ЁЁ3ЁЂИљОнБЛбѕЛЏЛђБЛЛЙдЕФГЬЖШВЛЭЌНјааХаЖЯ
ЁЁЁЁЁЁ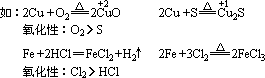
ЁЁ4ЁЂИљОнЗДгІЬѕМўХаЖЯ
ЁЁЁЁЁЁ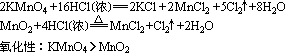
ЃЈШ§ЃЉГЃМћЕФбѕЛЏМСКЭЛЙдМСЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁГЃМћЕФбѕЛЏМСгаЃК Cl2ЁЂO2ЁЂSЁЂFe3ЃЋЁЂCu2ЃЋЁЂMnO2ЁЂKMnO4ЁЂK2Cr2O7ЁЂХЈH2SO4ЁЂHNO3ЕШЁЃ
ЁЁЁЁГЃМћЕФЛЙдМСгаЃК KЁЂNaЁЂMgЁЂFeЁЂFe2ЃЋЁЂClЃЁЂS2ЃЁЂCЁЂH2ЁЂSO2ЕШЁЃ
ЃЈЫФЃЉбѕЛЏЛЙдЗДгІЕФЙцТЩЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ1ЁЂЪиКуТЩ
ЁЁЁЁЛЏКЯМлгаЩ§БигаНЕЃЌЕчзггаЕУБигаЪЇЁЃЖдгквЛИіЭъећЕФбѕЛЏЛЙдЗДгІЃЌЛЏКЯМлЩ§ИпзмЪ§гыНЕЕЭзмЪ§ЯрЕШЃЌЪЇЕчзгзмЪ§гыЕУЕчзгзмЪ§ЯрЕШЁЃ
ЁЁ2ЁЂМлЬЌТЩ
ЁЁЁЁдЊЫиДІгкзюИпМлЃЌжЛгабѕЛЏадЃЛдЊЫиДІгкзюЕЭМлЃЌжЛгаЛЙдадЃЛдЊЫиДІгкжаМфМлЬЌЃЌМШгабѕЛЏадгжгаЛЙдадЃЌЕЋжївЊГЪЯжвЛжжаджЪЁЃЮяжЪШєКЌгаЖржждЊЫиЃЌЦфаджЪЪЧетаЉдЊЫиаджЪЕФзлКЯЬхЯжЁЃШч HClЃЌМШгабѕЛЏадЃЈгЩЧтдЊЫиБэЯжГіЕФаджЪЃЉЃЌгжгаЛЙдадЃЈгЩТШдЊЫиБэЯжГіЕФаджЪЃЉЁЃ
ЁЁ3ЁЂЧПШѕТЩ
ЁЁЁЁНЯЧПбѕЛЏадЕФбѕЛЏМСИњНЯЧПЛЙдадЕФЛЙдМСЗДгІЃЌЩњГЩШѕЛЙдадЕФЛЙдВњЮяКЭШѕбѕЛЏадЕФбѕЛЏВњЮяЁЃ
ЁЁЁЁ
ЁЁ4ЁЂзЊЛЏТЩ
ЁЁЁЁбѕЛЏЛЙдЗДгІжаЃЌвддЊЫиЯрСкМлЬЌМфЕФзЊЛЏзюШнвзЃЛЭЌжждЊЫиВЛЭЌМлЬЌжЎМфШєЗЂЩњЗДгІЃЌдЊЫиЕФЛЏКЯМлжЛППНќВЛНЛВцЃЛЭЌжждЊЫиЯрСкМлЬЌМфВЛЗЂЩњбѕЛЏЛЙдЗДгІЁЃ
ЁЁЁЁ
ЁЁ5ЁЂФбвзТЩ
ЁЁЁЁдНвзЪЇЕчзгЕФЮяжЪЃЌЪЇКѓОЭдНФбЕУЕчзгЃЌдНвзЕУЕчзгЕФЮяжЪЃЌЕУКѓОЭдНФбЪЇШЅЕчзгЁЃ
ЁЁЁЁвЛжжбѕЛЏМСЭЌЪБКЭМИжжЛЙдМСЯргіЪБЃЌЛЙдадзюЧПЕФЯШЗЂЩњЗДгІЃЛвЛжжЛЙдМСгіЖржжбѕЛЏМСЪБЃЌбѕЛЏадзюЧПЕФЯШЗЂЩњЗДгІЁЃ
Р§1ЁЂвбжЊЗДгІЃК2FeCl3ЃЋ2KI=2FeCl2ЃЋ2KClЃЋI2Ђй
2FeCl2ЃЋCl2=2FeCl3 Ђк
I2ЃЋSO2ЃЋ2H2O=H2SO4ЃЋ2HI Ђл
ЁЁЁЁ ХаЖЯЯТСаЮяжЪЕФЛЙдФмСІгЩДѓЕНаЁЕФЫГађЪЧ
ЁЁAЃЎIЃ>Fe2+>ClЃ>SO2ЁЁЁЁЁЁЁЁBЃЎClЃ>Fe2+>SO2>IЃ
ЁЁCЃЎFe2+>IЃ>ClЃ>SO2ЁЁЁЁЁЁЁЁDЃЎSO2>IЃ> Fe2+> ClЃ
Д№АИЃКD
НтЮіЃКЃЈ1ЃЉИљОнбѕЛЏЛЙдЗДгІЕФЙцТЩЃК
ЁЁЁЁЁЁ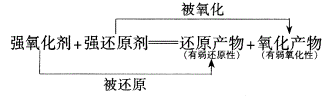
ЁЁЁЁЁЁбѕЛЏМСЕУЕчзгЕФЛЙдВњЮяЃЌОпгавЛЖЈЛЙдадЃЌЕЋЦфЛЙдадаЁгкЗДгІЮяжаЕФЛЙдМСЁЃгЩДЫПЩжЊЃЌИљОнЗДгІЗНГЬЪНПЩвдХаЖЯЛЙдФмСІЧПШѕЃКгЩЗДгІЂйПЩжЊЃКIЃ>Fe2+ЃЌЗДгІЂкПЩжЊЃКFe2+>IЃЃЌЗДгІЂлПЩжЊЃКSO2>IЃЃЌШ§епЕФЙиЯЕЮЊSO2>IЃ> Fe2+> ClЃЁЃ
Р§2ЁЂбѕЛЏЛЙдЗДгІЕФЬиеїЪЧЗДгІЧАКѓдЊЫиЕФЛЏКЯМлЗЂЩњИФБфЁЃИљОнетвЛЬиеїХаЖЯЯТСаЗДгІЪєгкбѕЛЏЛЙдЗДгІЕФЪЧЃЈЁЁЃЉ
AЃЎ2NaAlO2ЃЋCO2ЃЋ3H2O=2Al(OH)3Ё§ЃЋNa2CO3
BЃЎK2MnO4ЃЋCl2=2KClЃЋMnO2ЃЋO2
CЃЎK2MnO4ЃЋCl2=2KClЃЋ2Mn2O7
DЃЎ6NaAlO2ЃЋAl2(SO4)3ЃЋ12H2O=8Al(OH)3Ё§ЃЋ3Na2SO4
Д№АИЃКBЁЂC
НтЮіЃКгЩЛЏбЇЗДгІЧАКѓдЊЫиЛЏКЯМлЕФБфЛЏРДХаЖЯПЩжЊAЁЂDСНИіЗДгІЗНГЬЪНЃЌЗДгІЧАКѓдЊЫиЕФЛЏКЯМлОљУЛгаЗЂЩњБфЛЏЁЃBбЁЯюжаЛЏбЇЗДгІЗНГЬЪНжаMnдЊЫигЩЃЋ6МлБфЮЊЃЋ4МлЃЌбѕдЊЫигЩЃ2МлБфЮЊ0МлЃЌClдЊЫигЩ0МлБфЮЊЃ1МлЃЛCбЁЯюжаClдЊЫигЩЃЋ5МлЯТНЕжСЃ1МлЃЌMnдЊЫигЩЃЋ6МлЩЯЩ§жСЃЋ7МлЁЃ