|
一、一周知识概述
1、金属的通性;
2、镁、铝的物理性质及其用途;
3、镁和铝的化学性质;
4、铝的几种重要化合物的性质。
二、重难点解析
1、金属的通性
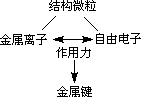
金属晶体:通过金属键结合而成的单质晶体。
金属键:金属离子跟自由电子之间存在的较强的作用,叫做金属键。
金属晶体中结构微粒:金属离子和自由电子。
●金属的物理性质:
状态:汞是液体,其余为固体。
颜色:大多为银白色,少数有特殊颜色,块状金属有金属光泽。
有延性和展性、导热性和导电性。
●金属的化学性质:M-ne-=Mn+
2、镁和铝的物理性质
(1)均为银白色金属,通常状态下为固体。具有金属的物理通性。
(2)密度较小,且ρ镁<ρ铝。
(3)熔点较低(相对其他金属而言),且镁比铝低。硬度较小,且镁比铝小。
3、镁和铝的化学性质
(1)与非金属反应
①和O2反应,常温下Mg、Al都能和O2反应,生成一层致密的氧化物保护膜。
 (耀眼白光、放出大量的热,生成白色固体) (耀眼白光、放出大量的热,生成白色固体)
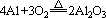 (没有镁那么容易,需在纯净的O2流中加热或在空气中加热到高温) (没有镁那么容易,需在纯净的O2流中加热或在空气中加热到高温)
②镁、铝除能跟氧气反应外,还能跟其他非金属如硫、卤素等起反应
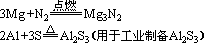
(2)与酸的反应
①与非氧化性酸(如盐酸、稀硫酸等)的置换反应
Mg+2H+=Mg2++H2↑,2Al+6H+=2Al3++3H2↑
上述反应也是氧化还原反应。
②与氧化性酸(如硝酸、浓硫酸等)的反应
铝在常温下遇浓硫酸、浓硝酸发生钝化,但加热时可以发生反应。镁可与硝酸、浓硫酸等发生反应,如:
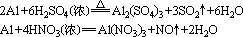
(3)与强碱的反应
铝和强碱溶液反应,不是铝直接和碱反应,而是铝先和强碱溶液中的水反应生成氢氧化铝,然后再和强碱反应生成偏铝酸盐。

标电子转移时就可以直接地理解铝和NaOH溶液反应的实质:

(4)与某些氧化物反应
①镁铝与水的反应
水和镁在常温下反应缓慢,加热时反应较快:
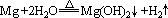
冷水和铝几乎不反应,跟沸水发生缓慢反应:
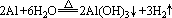
②镁可与CO2、SO2等反应

③铝热反应:铝与具有一定氧化性的金属氧化物在高温下的反应。
常见的氧化物有:Fe2O3、FeO、Fe3O4、CuO、MnO2、V2O5、Cr2O3、Co3O4、Co2O3等。反应的实质是氧化还原反应;反应的特点是在高温下进行,反应迅速放出大量的热,生成的新金属单质呈液态而与Al2O3分离;反应的实际应用是焊接钢轨和冶炼难熔金属如钒、铬、锰。
4、镁铝化合物的性质
(1)镁的重要化合物
①氧化镁(MgO)
a.化学性质
MgO+H2O=Mg(OH)2(自然界不存在MgO)
MgO+2HCl=MgCl2+H2O
MgO+2NH4Cl=MgCl2+2NH3↑+H2O
b.制备方法
工业上用煅烧菱镁矿来制取氧化镁:
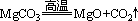
②氯化镁(MgCl2)
氯化镁的存在、提纯、用途可用如下框图概述:

①处反应是:Mg2++2OH-=Mg(OH)2↓
②处反应是:Mg(OH)2+2H+=Mg2++2H2O
③处理由是:防止MgCl2・6H2O在加热时水解产生Mg(OH)2或Mg(OH)Cl。
(2)铝的重要化合物
①Al2O3
a.Al2O3的主要物理性质及用途
Al2O3是白色固体,熔点高,是优良的耐水材料。
α―Al2O3俗称刚玉,硬度相当高,仅次于金刚石,可用作钟表轴承。
b.Al2O3的化学性质
氧化铝是典型的两性氧化物,新制备的氧化铝既能和酸反应,又能和碱反应:
Al2O3+6H+=2Al3++3H2O
Al2O3+2OH-=2AlO2-+2H2O
熔融的氧化铝是可以电解制铝的:
氧化铝不能直接和水反应生成氢氧化铝。
②氢氧化铝[Al(OH)3]
a.氢氧化铝的化学性质
Al(OH)3具有两性,可用电离平衡移动的原理来解释:氢氧化铝的电离方程式可表示如下:
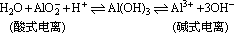
其电离程度相当微弱,只有加入强酸(或强碱)时,大量的H+(或OH-)才能破坏氢氧化铝的电离平衡,使平衡向右(或左)移动,生成铝盐(或偏铝酸盐),所以氢氧化铝既具有碱性,又具有酸性。当加入弱酸或弱碱时,因H+或OH-浓度太小,不能使上述平衡移动,因此Al(OH)3只溶于强酸或强碱,而不溶于弱酸或弱碱,如:
Al(OH)3+3HCl=AlCl3+3H2O
Al(OH)3+NaOH=NaAlO2+2H2O
b.氢氧化铝的制备
在实验室里,可用易溶的铝盐和氨水制氢氧化铝或在偏铝酸钠溶液中通入CO2,也可以让Al3+和AlO2-反应制得。有关反应为:
Al3++3NH3・H2O=Al(OH)3↓+3NH4+
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
或AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(CO2过量)
Al3++3AlO2-+6H2O=4Al(OH)3↓
- 返回 -
|