|
一、一周课程概述
本周讲述第一节和第二节的部分内容,包括 Cl2 的实验室制法, Cl2 的工业制法,氯离子的检验,卤素的原子结构特点,卤素单质的物理性质、化学性质。
二、重难点知识剖析
(一)、氯气的实验室制法
1 、反应原理
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O
(1) 离子方程式为 MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O
(2) 不能用稀盐酸,只能用浓盐酸,因为稀盐酸的还原性比浓盐酸弱。
(3)可用 KMnO4、KClO3、K2Cr2O7、Ca(ClO)2 等氧化剂来代替 MnO2,其中实验室常用 KMnO4 与浓 HCl 反应(不需加热)来快速制取少量 Cl2。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
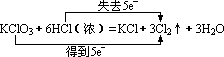
K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O
Ca(ClO)2+4HCl(浓)=CaCl2+Cl2↑+2H2O
2 、反应装置 固+液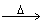 气 气
(1)气体发生装置使用的主要仪器有铁架台、酒精灯、圆底烧瓶、分液漏斗、导气管
(2)一套完整的制气装置应包括四个部分
3 、净化和干燥
用饱和食盐水吸收 Cl2 中的 HCl, 用浓 H2SO4 吸收 Cl2 中的 H2O(g) ,且吸收 HCl 在前,吸收 H2O(g) 在后。
4 、收集方法
(1)向上排空气法
(2)排饱和食盐水法(Cl2 在饱和食盐水中溶解度较小)
5 、验满
(1)湿润的 KI 淀粉试纸(若变蓝,则收集满了)
(2)湿润的蓝色石蕊试纸(若先变红,后褪色,则收集满了)
6 、尾气吸收
用 NaOH 溶液吸收多余的 Cl2:Cl2+2NaOH=NaCl+NaClO+H2O

(二)、氯气的工业制法
电解饱和食盐水 2NaCl+2H2O 2NaOH+H2↑+Cl2↑ 2NaOH+H2↑+Cl2↑
电解熔融的 NaCl 2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑
(三)、氯离子的检验
1 、试剂
AgNO3 溶液和稀 HNO3。其中稀 HNO3 的作用是排除 CO32-等的干扰。
2Ag++CO32-=Ag2CO3↓ Ag2CO3+2H+=2Ag++CO2↑+H2O
2 、原理
Ag++Cl-=AgCl↓ AgCl不溶于稀 HNO3
3 、方法
在被检测液中滴加 HNO3 酸化的 AgNO3 溶液 , 如产生白色沉淀,即可判断该溶液中含有 Cl-。
(四)、卤素的原子结构特点

注:砹(At)是放射性元素,一般不作研究。
相同点:最外层电子层上都有 7 个电子。
不同点:从 F 到 I ,核电荷数逐渐增多,电子层数逐渐增多,原子半径逐渐增大。
(五)卤素单质的物理性质
F2―淡黄绿色气体 Cl2―黄绿色气体
Br2―深红棕色液体 I2―紫黑色固体
1 、相似性
都有颜色和毒性,不易溶于水(除 F2 外),易溶于苯、四氯化碳等有机溶剂。下表列出了显色情况:

注:
(1)有机溶剂中密度比水小的有苯、汽油、酒精等,密度比水大的有 CCl4、CS2等。以上溶剂中只有酒精易溶于水,其余均难溶于水。
(2)溶液的颜色随浓度的增大而加深。
(3)上表所列颜色变化情况比较复杂,常说的颜色为:溴水为黄色,溴溶解在有机溶剂中为橙红色,碘水为黄色,碘溶解在苯、汽油、四氯化碳中为紫色,碘溶解在酒精中(即碘酒)为褐色。
2 、递变性
按 F2、Cl2、Br2、I2 的顺序,单质的颜色逐渐加深;状态由气态变化到液态,再变化到固态;熔、沸点逐渐升高;在水中的溶解度逐渐减小(F2除外)。
3 、特性
(1)液溴是深红棕色液体,且易挥发
液溴应密封保存,如果把溴存放在试剂瓶里,需加水液封,以减少挥发。盛溴的试剂瓶不能用橡皮塞(Br2 可腐蚀橡胶)。
(2)碘易升华―常用于分离、提纯I2
碘用棕色试剂瓶盛装,并放在阴凉处。
(六)卤素单质的化学性质
1 、与金属的反应
2Fe+3Cl2 2FeCl3 2FeCl3
2Fe+3Br2 2FeBr3 2FeBr3
Fe+I2 FeI2 FeI2
由铁元素的化合价可知:I2的氧化性比Cl2、Br2 都弱。
Zn+I2 ZnI2 ZnI2
现象:有紫烟生成。
原因:H2O作催化剂,反应放热,使碘升华。
2 、与氢气的反应
H2+F2=2HF(在暗处剧烈化合并发生爆炸)
H2+Cl2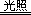 2HCl(光照条件下可发生爆炸) 2HCl(光照条件下可发生爆炸)
H2+Br2 2HBr(在 500 ℃时才能反应) 2HBr(在 500 ℃时才能反应)
H2+I2 2HI(不断 加热的条件下才能缓慢反应) 2HI(不断 加热的条件下才能缓慢反应)
(1)按 F2、Cl2、Br2、I2的顺序,它们与 H2 化合渐难
(2)生成物的 热稳定性

(3)可逆反应
正反应:向生成物方向进行的反应。
逆反应:向反应物方向进行的反应。
可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
例:H2+I2 2HI , 2HI ,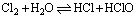 两个反应均为可逆反应。 两个反应均为可逆反应。
2H2+O2 2H2O , 2H2O 2H2O , 2H2O 2H2↑+O2↑这两个反应由于不在同一条件进行,故不是可逆反应。 2H2↑+O2↑这两个反应由于不在同一条件进行,故不是可逆反应。
3 、与水的反应
2F2+2H2O=4HF+O2
Cl2+H2O=HCl+HClO
Br2+H2O=HBr+HBrO
I2+H2O=HI+HIO
(1)按 F2、Cl2、Br2、I2 的顺序,它们与水反应剧烈程度逐渐减弱
(2)氢卤酸的酸性

4 、与碱的反应
2F2+2NaOH=2NaF+OF2↑+H2O
X2+2NaOH=2NaX+NaXO+H2O(X=Cl、Br、I)
X2+6KOH(浓) 5KX+KXO3+3H2O 5KX+KXO3+3H2O
5 、卤素单质间的置换反应
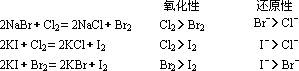
(1) F2 能与水反应放出 O2,故 F2 不能从卤素化合物的水溶液中置换出卤素单质
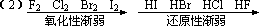
6 、碘与淀粉的反应――碘的特性
碘遇淀粉呈现特殊的蓝色,加热后蓝色消失,冷却后溶液又重新呈现出蓝色。
总结:卤素性质的相似性和递变性
1 、相似性
(1)卤素都呈现非金属性,单质具有一定的氧化性,均能与金属、非金属、水和碱溶液反应。
(2)常见的化合价有-1、0、+1、+3、+5、+7(氟无正价)

(3)均能形成气态氢化物(HX)
(4)最高价氧化物对应的水化物(HXO4)为酸(F 除外)
2 、递变性
按 F 、 Cl 、 Br 、 I 的顺序,元素的非金属性逐渐减弱,单质(X2)的氧化逐渐减弱,卤离子(X-)的还原性逐渐增强,卤化氢(HX)的还原性逐渐增强,单质(X2)与 H2 化合逐渐困难,气态氢化物(HX)的热稳定性逐渐减弱,最高价含氧酸(HXO4) [F 除外 ] 的酸性逐渐减弱,氢卤酸(HX)的酸性逐渐增强。
以上相似性、递变性的原因为卤素原子最外层的电子数为 7 ,且按 F、Cl、Br、I 的顺序,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的吸引力逐渐减弱。
- 返回 -
|